Kunci dan Jawaban
Kunci Jawaban IPA Kelas 9 Halaman 138-139, Kurikulum Merdeka
Berikut Adalah Kunci Jawaban IPA Kelas 9 Halaman 138-139, Kurikulum Merdeka, a) Dengan menggunakan bubuk magnesium maka reaksi dengan larutan asa
Penulis: M Fadli | Editor: M Fadli
TRIBUNJAMBI.COM - Berikut Adalah Kunci Jawaban IPA Kelas 9 Halaman 138-139, Kurikulum Merdeka
Jawaban:
Penjelasan Pengamatan
a) Dengan menggunakan bubuk magnesium maka reaksi dengan larutan asam berjalan lebih cepat dibandingkan dengan jika menggunakan pita magnesium.
Penjelasan:
Bubuk magnesium memiliki luas permukaan yang lebih besar dibandingkan dengan pita magnesium. Luas permukaan yang lebih besar akan meningkatkan jumlah tumbukan antara molekul magnesium dan molekul asam. Hal ini akan mempercepat reaksi kimia antara magnesium dan asam.
b) Reaksi antara kapur dengan asam klorida akan makin cepat apabila kita menggunakan asam klorida pekat.
Penjelasan:
Asam klorida pekat memiliki konsentrasi asam klorida yang lebih tinggi dibandingkan dengan asam klorida encer. Konsentrasi asam klorida yang lebih tinggi akan meningkatkan jumlah ion klorida yang tersedia dalam larutan. Ion klorida berperan sebagai katalisator dalam reaksi antara kapur dan asam klorida. Katalisator adalah zat yang dapat mempercepat reaksi kimia tanpa ikut bereaksi.
c) Reaksi antara seng dengan asam sulfat akan berjalan lebih cepat apabila ditambahkan beberapa tetes larutan tembaga (II) sulfat.
Penjelasan:
Larutan tembaga (II) sulfat mengandung ion tembaga (II). Ion tembaga (II) dapat bereaksi dengan ion seng dalam larutan asam sulfat untuk membentuk endapan tembaga. Endapan tembaga ini akan menutupi permukaan seng. Hal ini akan mencegah ion seng bereaksi dengan asam sulfat. Akibatnya, reaksi antara seng dan asam sulfat akan berjalan lebih cepat.
d) Makanan dapat dimasak lebih cepat dalam panci bertekanan tinggi dibandingkan panci biasa.
Penjelasan:
Panci bertekanan tinggi memiliki tutup yang rapat. Tutup yang rapat ini akan meningkatkan tekanan dalam panci. Peningkatan tekanan akan meningkatkan suhu titik didih air. Akibatnya, makanan akan lebih cepat matang.
e) Semakin banyak mengkonsumsi makanan dan minuman manis maka gigimu akan lebih cepat mengalami kerusakan.
Penjelasan:
Makanan dan minuman manis mengandung gula. Gula dapat diubah oleh bakteri di mulut menjadi asam. Asam ini dapat mengikis enamel gigi. Akibatnya, gigi menjadi lebih rentan terhadap kerusakan.
Penjelasan Pengikisan Batuan Kapur oleh Hujan Asam
a) Apabila tinggi puncak batuan saat ini adalah 6.000 cm, perkirakanlah tinggi gunung 5 juta tahun yang lalu ketika gunung ini terbentuk.
Penjelasan:
Kecepatan pengikisan batuan kapur oleh hujan asam adalah 1,7 cm setiap 1.000 tahun. Artinya, dalam 5 juta tahun, batuan kapur akan terkikis sebesar 5.000.000 cm / 1.000 = 5.000 cm.
Jadi, tinggi gunung 5 juta tahun yang lalu adalah 6.000 cm - 5.000 cm = 1.000 cm.
b) Bandingkanlah kecepatan pengikisan apabila gunung kapur ini terdapat di Alaska.
Penjelasan:
Kecepatan pengikisan batuan kapur oleh hujan asam akan lebih cepat di daerah yang memiliki curah hujan yang tinggi. Alaska memiliki curah hujan yang tinggi, sehingga kecepatan pengikisan batuan kapur oleh hujan asam di Alaska akan lebih cepat dibandingkan di Malaysia.
c) Jelaskan mengapa kecepatan pengikisan batuan kapur oleh hujan asam terjadi lebih cepat di tempat-tempat yang memiliki banyak pabrik dan industri.
Penjelasan:
Pabrik dan industri menghasilkan gas buang yang mengandung sulfur dioksida dan nitrogen oksida. Gas-gas ini dapat bereaksi dengan air di udara membentuk asam sulfat dan asam nitrat. Asam-asam ini dapat meningkatkan keasaman hujan. Hujan asam yang lebih asam akan lebih cepat mengikis batuan kapur.
Kesimpulan
Pengamatan-pengamatan di atas dapat dijelaskan dengan teori kinetika kimia. Menurut teori kinetika kimia, laju reaksi kimia dipengaruhi oleh beberapa faktor, yaitu:
Luas permukaan
Konsentrasi
Katalisator
Temperatur
Tekanan
Dalam kasus pengamatan di atas, faktor-faktor yang mempengaruhi laju reaksi kimia adalah:
Luas permukaan (a, b, c)
Konsentrasi (b, c)
Katalisator (c)
Temperatur (a, b, c)
Tekanan (d)
Dengan memahami faktor-faktor yang mempengaruhi laju reaksi kimia, kita dapat mengendalikan laju reaksi kimia untuk tujuan tertentu.
Baca juga: Kunci Jawaban IPA Kelas 9 Halaman 134-35, Kurikulum Merdeka
Baca juga: Kunci Jawaban IPS Kelas 9 Halaman 159, Diskusi Jigsaw
Baca juga: Kunci Jawaban IPS Kelas 9 Halaman 159, Proyek Strategis Nasional
Disclaimer
1. Pembahasan di atas hanya sebagai referensi belajar.
2. Soal di atas merupakan pertanyaan terbuka. Artinya ada beberapa jawaban tidak terpaku di atas.
3. Artikel ini tidak mutlak menjamin kebenaran jawaban. Siswa dapat mengembangkan jawaban yang lebih baik.
Sumber Buku:
Cece Sutia,dkk,
Penerbit
Pusat Perbukuan
Badan Standar, Kurikulum, dan Asesmen Pendidikan
Kementerian Pendidikan, Kebudayaan, Riset, dan Teknologi
Kompleks Kemdikbudristek Jalan RS. Fatmawati, Cipete, Jakarta Selatan
https://buku.kemdikbud.go.id
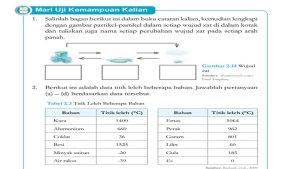
| Kunci Jawaban IPA Kelas 7 Halaman 60 : Perubahan Wujud Zat |
|
|---|
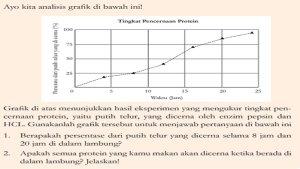
| Kunci Jawaban IPA Kelas 8 Halaman 52, Kurikulum Merdeka: Pencernaan Protein |
|
|---|
| Kunci Jawaban IPS Kelas 7 Halaman 38 : Lalu Lintas |

|
|---|
| Kunci Jawaban Bahasa Inggris SMP Kelas 9 Halaman 36 : Worksheet 1.4 |

|
|---|
| Kunci Jawaban PAI Kelas 8 Halaman 252, Menuntut Ilmu |

|
|---|















Isi komentar sepenuhnya adalah tanggung jawab pengguna dan diatur dalam UU ITE.